Laboratorios de Investigación Básica
Cardioprotección y factores de riesgo cardiovascular
Neurocardiología
Patología experimental
Laboratorios de Investigación Básica y Traslacional
Laboratorio de mecánica cardíaca y remodelamiento ventricular
Director del laboratorio: Dr. Martín Donato.
Integrantes:
- Dra. Eliana Bin, (Jefa de Trabajos Prácticos, Facultad de Ciencias Médicas - UBA)
- Est. Lautaro Córdoba, (Estudiante de Medicina, UBA)
Estudio de los efectos del condicionamiento isquémico remoto sobre el remodelamiento ventricular post-infarto de miocardio
Resumen:
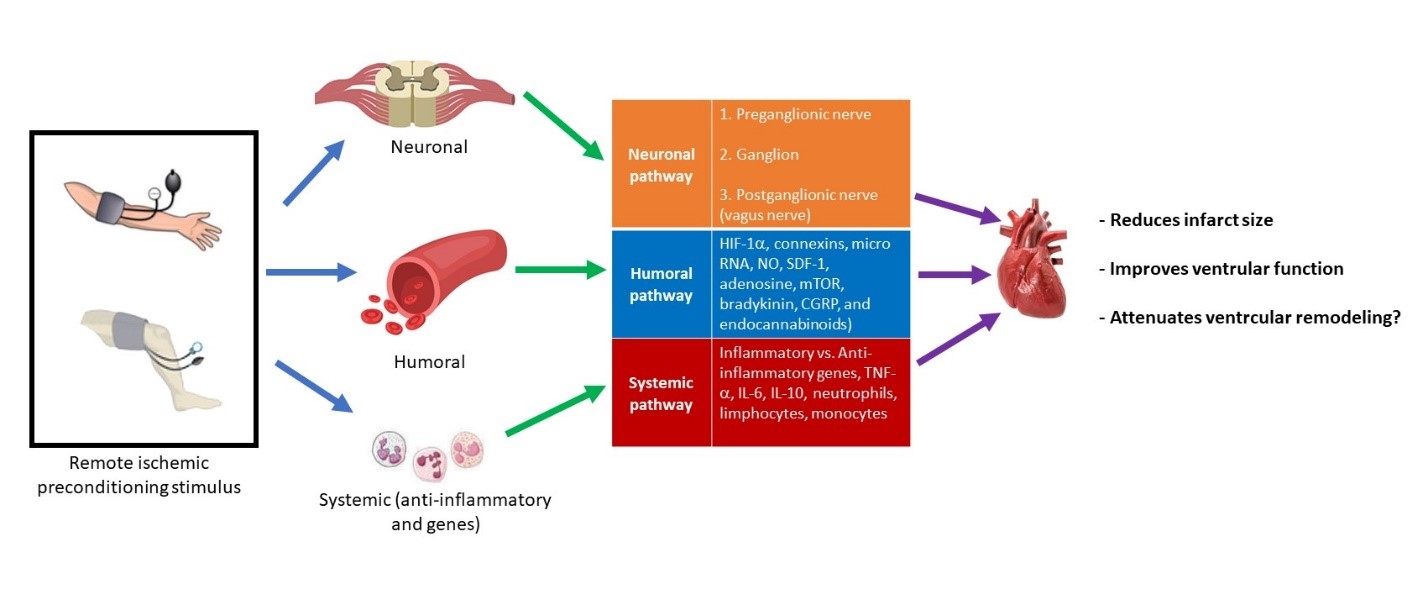
Las enfermedades cardiovasculares son la causa más frecuente de morbimortalidad, invalidez y pérdida de la capacidad laboral en adultos en el mundo y también en nuestro país. Particularmente, el infarto agudo de miocardio (IAM) es una de las patologías que más desafíos le impone al sistema de salud. El diagnóstico temprano permite adoptar estrategias para reperfundir el miocardio (fibrinolíticos o angioplastia transluminal coronaria primaria). Sin embargo, por múltiples razones, un número significativos de pacientes no acceden a una terapia de reperfusión o la misma es insatisfactoria. Basado en estos conceptos, es necesario asociar a estos tratamientos alguna estrategia que reduzca el daño ocasionado por el infarto. En este sentido, el precondicionamiento isquémico remoto (PCr) surge como una opción con posible extrapolación clínico-quirúrgica. El PCr es un fenómeno por el cual breves episodios de isquemia/reperfusión realizados en un tejido u órgano alejado del corazón reducen el tamaño de infarto producto de un episodio de isquemia prolongado en el corazón. Una limitación de esta estrategia es el hecho de tener que realizar los episodios de isquemia/reperfusión antes de la isquemia miocárdica prolongada. Razón por la cual, en el año 2005, Kerendi y col demuestran que breves episodios de isquemia y reperfusión de la arteria renal, realizados al mismo momento que la reperfusión miocárdica eran capaces de reducir el tamaño del infarto de miocardio, un fenómeno denominado postcondicionaminto isquémico remoto (PostCr). Siendo este mecanismo de protección más extrapolable al ámbito clínico.
Si bien en los últimos años se han estudiado los mecanismos que explican ambos fenómenos de protección, su estudio se ha focalizado en la secuencia de eventos intracelulares que ocurren en la reperfusión miocárdica temprana y son escasos los trabajos que evaluaron el efecto de estas estrategias sobre el remodelamiento ventricular postinfarto de miocardio. Esto es de relevancia, ya que el proceso de remodelamiento ventricular condiciona la evolución de los pacientes que sufren un IAM, por lo tanto, limitar el remodelado ventricular es relevante ya impacta directamente en la evolución clínica de los pacientes.
En consecuencia, el objetivo de nuestra línea es evaluar si el PCr y el PostCr atenúan el remodelamiento ventricular izquierdo y retrasan la evolución a la insuficiencia cardíaca modificando la respuesta inflamatoria, incrementando la neovascularización, modificando la composición de la cicatríz y el remodelamiento de la zona no infartada independientemente de su efecto sobre el tamaño de infarto.
Laboratorio de cardioprotección y factores de riesgo cardiovascular.
Director del laboratorio: Dra. Verónica D’Annunzio
Integrantes:
- Dra. Virginia Pérez, (Investigadora asistente CONICET, Jefa de Trabajos Prácticos, Facultad de Ciencias Médicas - UBA)
- Dra. Tamara Zaobornyj, (Investigadora asistente CONICET, Jefa de Trabajos Prácticos, Facultad de Farmacia y Bioquímica - UBA)
- Eugenia Godoy Olazar, (Becaria doctoral UBA)
- Fernando García, (Médico, UBA con Beca Peruilh)
- Candela Noir, (Estudiante de Medicina, UBA)
Mecanismos de proteccion miocardica frente a la injuria por isquemia/reperfusión en modelos experimentales con comorbilidades: rol del estrés oxidativo
Resumen:
Las enfermedades cardiovasculares son la primera causa de muerte en nuestro país, y particularmente el infarto agudo de miocardio (IAM) se asocia a factores de riesgo tales como la dislipidemia y el envejecimiento. Si bien nadie duda que las terapias de reperfusión son el mejor tratamiento para el IAM, bajo ciertas condiciones genera daño conocido como lesión por reperfusión, donde el aumento del estrés oxidativo juega un rol principal en la generación del daño. Es por eso que desde hace varias décadas investigadores básicos y clínicos han desarrollado estrategias cardioprotectoras fisiológica, tales como los protocolos de condicionamiento (pre y poscondicionamiento) y el ejercicio; y farmacológicas para atenuar los daños producidos por la isquemia/reperfusión. Sin embargo, estas estrategias no han sido del todo exitosas en el ámbito clínico, quizás debido a que la mayoría de los estudios en modelos animales experimentales fueron realizado en animales jóvenes y sanos. Es por ello que resulta de vital importancia utilizar modelos animales experimentales con envejecimiento y con dislipidemia producida con una dieta alta en grasas, entre otros, para el estudio de estos mecanismos de protección miocardica.
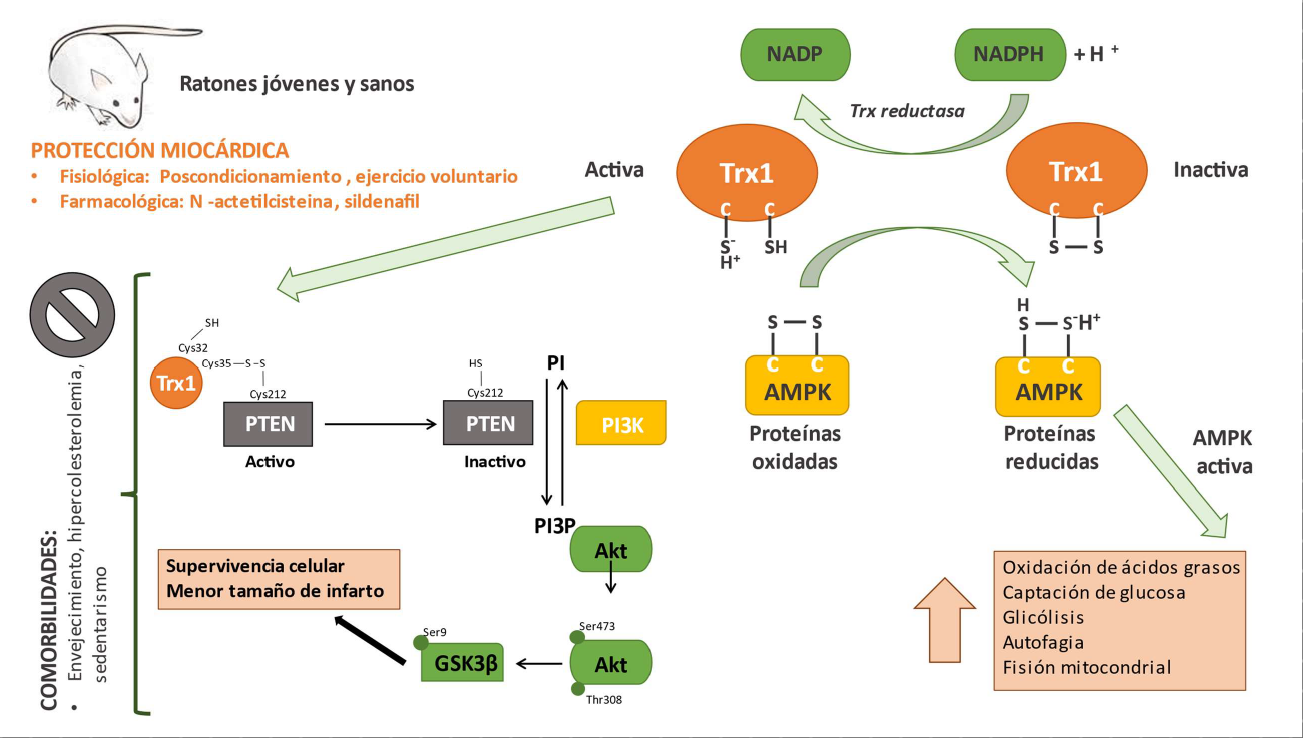
Como fue mencionado el estrés oxidativo es un blanco de estudio importante en la lesión por injuria/reperfusión y además genera daño per se en situaciones de comorbilidad como la dislipidemia y el envejecimiento. Es por ello que estudiamos el rol del sistema de tiorredoxina que es uno de los sistemas antioxidantes celulares más importantes conocido hasta la actualidad. Particularmente la tiorredoxina-1 (Trx1) ha sido la más estudiada, y es una pequeña proteína (12KD) que tiene efectos anti apoptóticos, anti inflamatorios y ejerce efectos protectores frente a la injuria por isquemia/reperfusión.
En consecuencia, el objetivo de esta línea de investigación es estudiar el rol de la Trx1 ante la intervención de terapias cardioprotectoras fisiológicas (ejercicio voluntario) y farmacológicas (sildenafil, N-acetilcisteína) frente a la injuria por isquemia/reperfusión, estudiando los mecanismos intracelulares y mitocondriales involucrados en modelos experimentales con envejecimiento y/o dislipidemicos. Estos protocolos son realizados en modelos experimentales con dislipidemia experimental y/o envejecidos en ratones no transgénicos y en ratones transgénicos que sobreexpresan la Trx1 y la Trx1 inactiva.
Laboratorio de neurocardiología
Director del laboratorio: Dr. Bruno Buchholz
Integrantes:
- Dra. Verena Franco Riveros, (Becaria Postdoctoral CONICET, Jefa de Trabajos Prácticos, Dpto. de Anatomía, Facultad de Ciencias Médicas - UBA)
- Méd. Ignacio Barbieri, (Becario Doctoral UBA, Jefe de Trabajos Prácticos, Dpto. de Anatomía, Facultad de Ciencias Médicas - UBA)
- Ing. Eduardo Bernatené, (Profesional de Apoyo del CONICET)
- Srta. Sol Hernández Cicale, (Estudiante de Medicina, UBA)
- Srta. Suin Kim, (Estudiante de Medicina, UBA)
- Srta. Victoria Fernanda Ramírez Muñoz, (Estudiante de Medicina, UBA)
Neurocardiología experimental y traslacional: interacción cerebro–corazón, regulación autonómica y bases morfológicas de la neuromodulación
Resumen:
Nuestra línea de investigación estudia cómo el sistema nervioso autónomo participa en la lesión isquémica y en los procesos de reparación del corazón y del cerebro. Desde una perspectiva de neurocardiología experimental y traslacional, abordamos al eje cerebro–corazón como una red bidireccional en la que mecanismos autonómicos, inflamatorios y estructurales influyen de manera decisiva sobre la evolución de la enfermedad. Uno de nuestros principales objetivos es comprender cómo la modulación autonómica, en particular mediante estimulación vagal, puede inducir cardioprotección frente al infarto agudo de miocardio. Hemos demostrado que esta intervención reduce el tamaño del infarto y activa mecanismos comparables a los del precondicionamiento y postcondicionamiento isquémicos. Actualmente estudiamos la evolución temporal de estos efectos protectores, sus mecanismos neuroinmunes y su impacto sobre el remodelado ventricular y la progresión hacia la insuficiencia cardíaca.
Otro eje central del grupo es el estudio de la interacción cerebro–corazón en el contexto del accidente cerebrovascular (ACV) isquémico y del infarto de miocardio. Investigamos cómo la lesión cerebral aguda puede inducir alteraciones cardíacas funcionales, eléctricas y autonómicas, y cómo la lesión cardíaca isquémica puede asociarse a cambios conductuales, emocionales y cognitivos. En particular, estudiamos la relación entre infarto, remodelado cardíaco y alteraciones de la conducta, incluyendo ansiedad, depresión y trastornos de la memoria, así como los mecanismos autonómicos e inflamatorios involucrados. De manera complementaria, desarrollamos una línea de investigación morfológica orientada al estudio anatómico y microanatómico del sistema nervioso autónomo. Analizamos ganglios, plexos y nervios autonómicos, sus variaciones estructurales y sus relaciones topográficas, con especial interés en sus implicancias para la neuromodulación y los abordajes intervencionistas. En este marco, el estudio de la microanatomía del nervio vago ocupa un lugar relevante dentro del programa, como base para el diseño de estrategias terapéuticas más precisas y con mayor proyección traslacional.
En conjunto, nuestros estudios proponen al sistema nervioso autónomo como un eje integrador entre lesión, inflamación, remodelado y función en el corazón y el cerebro. Este enfoque busca generar conocimiento original sobre mecanismos fisiopatológicos y, al mismo tiempo, contribuir al desarrollo de nuevas estrategias terapéuticas en cardiopatía isquémica, stroke y neuromodulación.
Laboratorio de Patología Experimental
Directora del laboratorio: Dra. Georgina P. Ossani
Integrante:
- Gabriel Casas, (Especialista en Patología. Jefe de Trabajos Prácticos, Facultad de Ciencias Médicas - UBA. Tesista doctoral)
Efectos del litio sobre el hipocampo y el riñón en el tratamiento del trastorno bipolar
Resumen:
La patología constituye un puente entre la medicina básica y la medicina clínica, desempeña un papel fundamental en la investigación médica y el desarrollo de nuevas terapias. Al estudiar las características morfológicas y moleculares de los tejidos, los patólogos contribuyen a la comprensión de los mecanismos subyacentes de la enfermedad y al descubrimiento de biomarcadores y dianas terapéuticas. Este conocimiento impulsa el desarrollo de tratamientos más específicos y eficaces, lo que mejora los resultados clínicos y la calidad de vida de los pacientes.
El trastorno bipolar (TBP) es una enfermedad crónica y recurrente, de alta prevalencia (2-5%), que fue identificada por la OMS como la sexta causa de discapacidad en el mundo (Murray y Lopez, 1996). El litio fue aprobado en la década del 70 para la terapéutica del TBP, y aún hoy se considera como una droga de primera línea para el tratamiento de las diferentes fases de este desorden (Yatham y cols, 2013). El litio impacta por un lado en el hipocampo, estructura en la cual podría desempeñar un rol en la terapéutica del trastorno bipolar y, por otro lado, en el riñón, órgano en el cual tendría un efecto adverso que podría llevar al desarrollo de una enfermedad renal crónica.
En consecuencia, el objetivo general de nuestras líneas es emplear los recursos que brinda la patología para el estudio y la mayor comprensión del impacto del litio en los dos órganos mencionados, usando un modelo animal de administración crónica de esta sal. En el hipocampo, los objetivos particulares son estudiar el tamaño de neuronas piramidales en diferentes áreas y arborizaciones dendríticas y; en el riñón, describir la cronología de cambios y estimar la asociación entre los niveles de biomarcadores y marcadores tradicionales de inujuria renal, cuantificar la expresión de marcadores inmunohistoquímicos de lesión renal y estudiar el rol del canal epitelial de sodio.
Laboratorios de Investigación Clínica
Laboratorio de estudio de los síndromes coronarios agudos
Director del laboratorio: Dr. Ricardo Pérez de la Hoz
Integrantes
- Méd. Sandra Swieszkowski
- Méd. Martin Aladio
- Méd. Diego Costa
- Méd. Alejo Pérez de la Hoz
Resumen
Las enfermedades cardiovasculares (ECV) son la principal causa de discapacidad y de muerte en todo el mundo. La tasa de mortalidad por ECV ha presentado una clara tendencia negativa desde mediados del siglo XX. Recientemente algunos autores demostraron un enlentecimiento de dicha tendencia como consecuencia de una ralentización del descenso de la mortalidad por cardiopatía isquémica y un aumento de la mortalidad por insuficiencia cardíaca (IC). Esto redunda en un aumento de la supervivencia de estos pacientes, que han sufrido isquemia y necrosis miocárdica, que los predispone al remodelado cardíaco (RC) adverso o patológico, que deriva en insuficiencia cardiaca (IC).
El remodelamiento cardíaco se define como un cambio en la geometría del corazón, producto de modificaciones a nivel genético, molecular y celular que se manifiestan, como cambios en el tamaño, la forma y la función del corazón. Su determinante más importante es el tamaño del infarto y algunos de los factores que participan en el proceso de remodelamiento son la necrosis, la inflamación y el estrés oxidativo. Vale destacar a las metaloproteasas de matriz (MMP), no sólo porque degradan los componentes necróticos de la matriz extracelular, para que luego se deposite nuevo colágeno, si no que además son uno de los componentes más estudiados del RC.
El remodelamiento se desarrolla en 30-48% de los pacientes con IAM con elevación del segmento ST, y en un número considerable de pacientes con IAM sin elevación del segmento ST, pese a la utilización de los mejores tratamientos actualmente disponibles. Hoy las herramientas con las que contamos para atenuar el RC son la reperfusión, los IECAs, los β-bloqueantes y los antagonistas de mineralocorticoides. Vale aclarar que algunos de los estudios que sustentan estas recomendaciones datan del siglo pasado y que los más recientes cumplen casi dos décadas, lo que nos insta a trabajar en este tema.
El SCA desencadena una respuesta inflamatoria aguda y una respuesta de estrés. Sabemos que un mayor grado de inflamación se asocia con peor evolución en los pacientes. Nosotros recientemente describimos que esta mala evolución también se relaciona con los niveles plasmáticos de cortisol.
Cada vez son más los estudios que demuestran que “modular” la inflamación luego del SCA resulta beneficioso. Con los glucocorticoides sucede algo más complejo, ya que han demostrado tanto efectos beneficiosos como negativos, por lo que actualmente se desaconseja su uso en el SCA. Debemos destacar la complejidad de sus mecanismos de acción (génicos y no génicos), que son capaces de unirse a receptores de glucocorticoides (GR) y de mineralocorticoides (MR) y que mucha de la evidencia respecto de su uso en el IAM surge de trabajos realizados hace mucho tiempo, en ausencia de las terapias actuales. Hay quienes proponen que parte del beneficio de la eplerenona sobre el RC podría deberse al bloqueo de la acción de los glucocorticoides endógenos sobre el MR.
Por todo lo expuesto, resulta trascendente evaluar el remodelamiento ventricular en relación con el estrés y la inflamación en pacientes con SCA y animales con IAM experimental.

